FeLV – kočičí leukemie
Úvod
Virus kočičí leukemie (FeLV) patří mezi běžné infekční onemocnění u koček s prevalencí v USA 2 % – 30 %, v Evropě do 10 %. Riziko infekce je vyšší u dospělých samců žijících venku. Původcem FeLV je γ-retrovirus a nemoc je podobná FIV, kde je původcem příbuzný lentivirus.
V ne tak dávné minulosti byla FeLV považována za jednu z nejčastějších příčin úmrtí u koček (v důsledku onemocnění) a byla odpovědná až za třetinu úmrtí spojených s neoplazií. I když v poslední době incidence onemocnění klesla, neklesla její klinická důležitost a při komorbiditách je FeLV nejpravděpodobnější příčinou fatální prognózy. Průměrná přežitelnost u FeLV + koček v progresivní fázi onemocnění je 2,4-3,1 let, přičemž 80 % koček se nedožije více než 3 let od diagnózy.
Virus se přenáší vertikálně a horizontálně (zejména slinami, popsán je i přenos stolicí a močí). V prostředí je labilní, pro přenos je proto nutný těsný kontakt (např. krmení ze stejné misky).
FeLV je chronické onemocnění s dlouhou asymptomní fází. Z hlediska statusu rozlišujeme několik nosičství a během posledních let byl jejich původní systém vzhledem k novým informacím aktualizován. Zásadní změnou je, že antigen negativní, provirus pozitivní kočky jsou považovány za nositele FeLV viru a může u nich dojít k reaktivaci a vylučování viru. Že jste zjistili, že si biologii retrovirů nepamatujete?
Na úvod tedy krátké mikrobiologické okénko: Virus FeLV se skládá ze ssRNA nesoucí tři esenciální geny kódující proteiny a enzymy pro tvorbu virionů. Po vstupu viru do buňky jsou vyloučeny dvě kopie ssRNA a virová RNA-dependentní DNA polymeráza vytvoří DNA kopii virového genomu (tj. provirus), který je integrován do DNA buňky. Provirus je odpovědný za tvorbu nových virionů. Ve skutečnosti je FeLV skupina příbuzných virů a tvorba nových variant je vzhledem k absenci kontrolních funkcí nasnadě. Rozlišujeme tři základní skupiny: A, B a C, které se liší v biologii a tropizmu – skupina A je přenášena mezi kočkami, zatímco skupina B a C vzniká ze skupiny A rekombinací a mutací. Viry skupiny C odpovědné za fatální neregenerativní anémii jsou vzácné. Skupina B, která může být přenesena se skupinou A zvyšuje riziko rozvoje lymfomu. Existuje i skupina FeLV-T spojena s imunosupresní nemocí. Pokud životní cíle FeLV viru zjednodušíme, tak jim jde o transformaci buněk směrem k přežití. Jelikož jsou v dosahování tohoto cíle výbornými spojenci proto-onkogeny, tj. geny kódující např. růstové hormony, proteinkinázy, receptory pro růstové hormony atd., FeLV rádo dosahuje dysregulací těchto genů pro společný cíl, kterým je nadměrná buněčná proliferace.
Formy FeLV
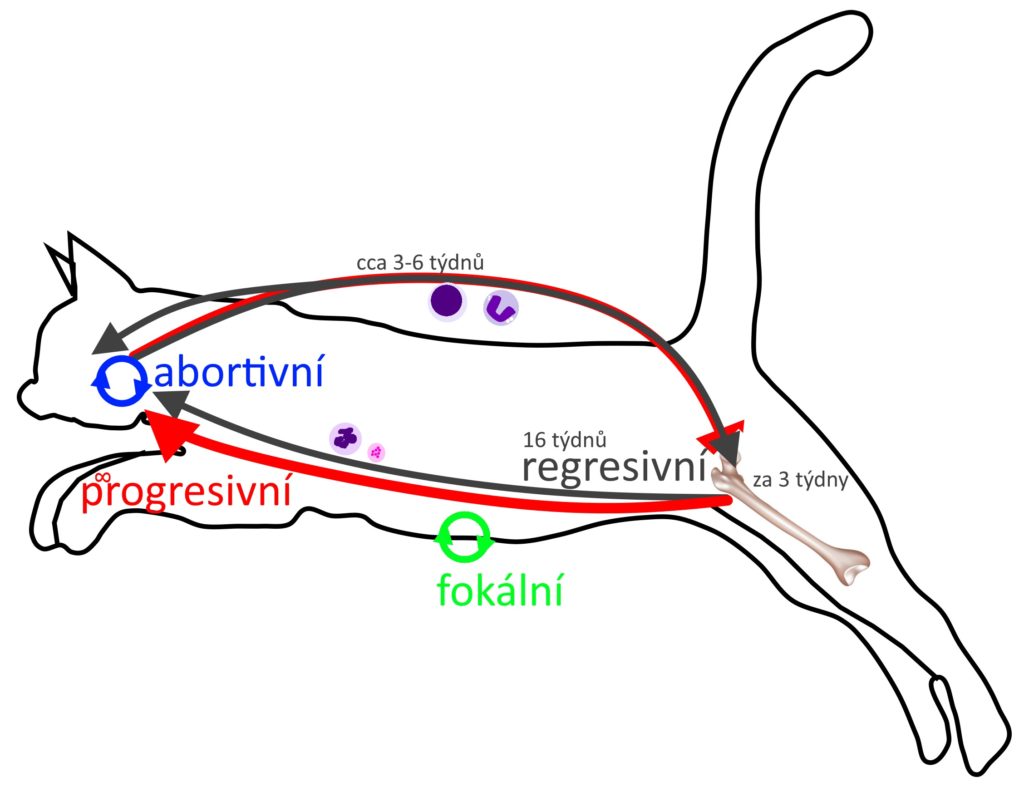
Z hlediska chování viru v organismu rozlišujeme čtyři typy onemocnění:
- abortivní infekci,
- regresivní infekci,
- progresivní infekci a
- fokální/atypickou infekci.
Abortivní infekce probíhá následovně: po vstupu do organismu se virus množí v lokální lymfatické tkáni v orofaryngeální oblasti. U některých koček může dojít v důsledku aktivace humorální a celulární imunity k zastavení infekce, zvíře tedy neprochází do viremické fáze. Zvířata mají vysoké titry neutralizačních protilátek, další markery se v krvi nenachází. Předpokládá se, že tento průběh je možný pouze u velmi malé infekční dávky a je možné, že v přirozených podmínkách k němu ani nedochází.
U regresivní infekce (1-10 % koček) dochází k replikaci viru a viremii před nebo těsně po infekci kostní dřeně. Po iniciální infekci se virus šíří prostřednictvím mononukleárů a tato viremie obvykle trvá týdny až měsíce. Během ní kočky virus vylučují. Po zhruba třech týdnech viremie dochází k infekci kostní dřeně a z infikovaných prekurzorových hematopoetických buněk vznikají infikované cirkulující granulocyty a trombocyty. Část koček je schopna ukončit viremickou fázi, není však schopna eliminovat virus z těla, jelikož je provirová DNA již v kmenových buňkách kostní dřeně. Při dělení buněk se provirová DNA dostává i do dcérskych buněk, nedochází však k transkripci a translaci proteinů. Tento stav se označuje jako „latentní infekce“ a nemusí být trvalý, při stimulu (např. imunosuprese) může znovu dojít k produkci virových partikulí.
U progresivní infekce nedochází k útlumu viru, ale naopak enormní replikaci v primárních lymfatických tkáních, kostní dřeni i slizničních tkáních. Kočky jsou permanentně viremické a vylučují virus do prostředí. Regresivní a progresivní infekci je tedy možné odlišit pomocí laboratorní diagnostiky, v některých případech je to však možné až za 4 měsíce od iniciálního vyšetření.
Fokální infekce se vyskytuje u cca 10 % experimentálně infikovaných koček a v přirozených podmínkách je pravděpodobně vzácná. Je charakterizována perzistentní atypickou replikací viru vedoucí k přerušované nebo snížené produkci antigenu.
Klinické příznaky
Klinické příznaky rozvíjející se po dlouhé asymptomní fázi jsou variabilní. Vzhledem k názvu onemocnění bychom předpokládali, že dominantním příznakem bude leukemie, avšak nejčastějším příznakem je anémie nebo komplikace spojené s imunosupresí. Z hlediska četnosti výskytu klinických příznaků se vyskytují u 15 % zvířat právě komorbidity (např. FIV, FIP, respirační infekce, mykoplasma, stomatitidy), u 11 % zvířat anémie, a u 10 % pacientů jsou přítomny malignity (lymfom, myeloproliferativní onemocnění).
Klinické projevy a prognóza onemocnění závisí od interakce mezi hostitelem a virem. Zdá se, že nejdůležitějším faktorem charakteru onemocnění je věk zvířete. Čerstvě narozená zvířata obvykle trpí atrofií brzlíku, která vede k závažné imunosupresi a následné smrti jedince. Čím je kočka starší, tím mírnější průběh můžeme očekávat. Staré kočky trpí nejčastěji abortivní nebo regresivní formou, pokud se u nich rozvine progresivní forma, jsou příznaky mírné a nástup onemocnění pozvolnější.
FeLV pozitivní kočky mají 62x větší pravděpodobnost rozvoje onkologického onemocnění než neinfikované kočky a nejčastějším tumorem je T-buněčný lymfom. Virus je považován za onkogen a jeho role v onkogenezi je jednoznačná, s postupem času a s poklesem incidence onemocnění se mění proporce zvířat s tumory a FeLV pozitivitou. Tyto statistiky jsou aktuálně kontroverzní, jelikož s novými metodami detekce viru v organismu se ukazuje, že i zvířata, která byla označena jako FeLV negativní, nosila ve skutečnosti provirus v DNA.
Vznik malignit u koček s FeLV je výsledkem různých mechanismů na úrovni buněčné proliferace. Nejdůležitějším mechanismem je inzerce proviru do DNA v blízkosti onkogenů, vedoucí k následné expresi (tvorbě) daného genu. Tento proces se označuje jako inzerční mutageneze. Inzerční mutageneze je příčinou zhruba třetiny případů rozvoje lymfomu koček.
Fibrosarkomy vyskytující se u FeLV koček jsou způsobeny virem kočičího sarkomu (FeSV), což je rekombinantní virus vznikající (de novo) z FeLV-A genomu a buněčných onkogenů. Během rekombinace FeSV získává jeden či více onkogenů schopnost, způsobit po krátké inkubační době multifokální tumory. Přítomnost FeSV je podmíněna infekcí FeLV, jelikož FeSV potřebuje k replikaci proteiny kódované virem FeLV. Tento typ fibrosarkomů postihuje mladé kočky, vzniká rychle, mnohočetně a často metastázuje do plic. Solitérní, pomalu rostoucí, lokálně invazivní fibrosarkomy u starších koček, obvykle klasifikovány jako FISS (feline injection site sarcoma), způsobené granulomatózní zánětlivou reakcí v místě aplikace (zejména vakcín s obsahem adjuvans), nemají spojitost s FeLV statusem zvířete.
Kromě onkologické symptomatologie způsobuje virus FeLV myelosupresi, která se projevuje anémií (regenerativní (10 %), neregenerativní),neutropenií (perzistentní, přechodnou nebo cyklickou), abnormalitami trombocytů a aplastickou anémií nebo pancytopenií. Myelosuprese je spojena s aktivní replikací viru a v patogenezi jednotlivých cytopenií může hrát signifikantní roli i imunitní složka v důsledku např. exprese cizích antigenů na povrchu FeLV infikovaných buněk. Myelosuprese vzniká samozřejmě i následkem hematologických malignit (leukemie, myelodysplastický syndrom, myelofibróza).
Další skupinou příznaků jsou neurologické příznaky (asi u 5 % koček s FeLV jsou dominantní), které mohou být způsobeny lymfomem, lymfocytární infiltrací v mozku a míše nebo přímou neurotoxicitou. Za podklad neurotoxicity se považuje zvýšení volného intracelulárního vápníku virovými glykoproteiny. Mezi klinické příznaky patří anizokorie, mydriáza, centrální slepota, Hornerův syndrom, vokalizace, hyperestezie, progresivní paralýza nebo inkontinence.
Další skupina příznaků u koček s FeLV je méně specifická, zahrnuje sekundární infekce, imunodeficienci a nebo imunitně-zprostředkovaná onemocnění. Jelikož si pod těmito termíny nedokážete asi úplně přesně představit, o co se jedná, tak jenom ve zkratce pár informací a pak se vrhneme na frustrující fascinující diagnostiku.
Co přesně je příčinou imunodeficience u FeLV se zatím přesně neví, tedy kromě očividných nálezů kterými jsou atrofie thymu, lymfopenie, neutropenie, snížená schopnost chemotaxe a fagocytózy nebo snížená aktivita komplementu. Následkem tohoto narušení imunitního systému jsou FeLV+ kočky vděčným cílem různých bakteriálních, virových, protozoálních a plísňových onemocnění. Mimo to je také narušena odpověď na vakcinaci, proto pokud nutně potřebujeme FeLV+ kočku vakcinovat, je vhodné vakcinovat častěji (např. každých 6 měsíců).
Navzdory imunosupresi mohou kočky trpět následky imunitně-zprostředkovaných onemocnění. Nejčastěji se setkáváme s nadprodukcí gamaglobulinů, které mohou indukovat tvorbu imunokomplexů s následnou glomerulonefritidou, polyartritidou, uveiditou nebo vaskulitidou.
Spektrum klinických příznaků je tedy opravdu pestré a vzhledem k výskytu komorbidit, není překvapivé, že při vstupním vyšetření nemocné kočky rádi sáhneme po rychlotestu, abychom FeLV jako příčinu vyloučili. Ale opravdu nám rychlotesty umožní spolehlivě identifikovat probíhající onemocnění?
Diagnostika
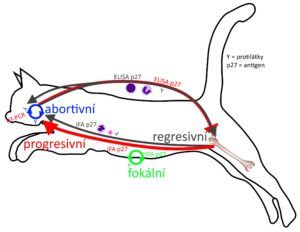
Možnosti detekce jednotlivých forem FeLV. Barva metody souhlasí s barvou formy.
V rámci laboratorní diagnostiky máme možnost detekovat následující markery: antigen p27, protilátky, RNA a provirus (DNA).
Nejprve tedy ve zkratce jak to zhruba v těle probíhá. Pokud se jedná o abortivní infekci, kde neprobíhá viremie, byl virus zdolán lokálně za pomocí protilátek. Jediná alterace budou tedy pozitivní titry protilátek. Jakmile se dostane virus do krve a chvíli zde pobývá, začne iniciovat produkci antigenu p27, který jsme zatím schopni detekovat jen volný v plazmě. Po usídlení v kostní dřeni dojde k produkci neutrofilů a trombocytů s antigenem p27 v buňce. Do tohoto momentu se mohou stát dvě věci – kočka začne tvořit protilátky a infekce se z periferie eliminuje (tj. regresivní infekce, kde můžeme a nemusíme mít pozitivní antigen p27, pozitivní PCR z krve či kostní dřeně, pozitivní protilátky) a nebo proti FeLV nedokáže bojovat a je v progresivní fází (enormní množství p27, vysoká nálož RNA a DNA detekovaná pomocí PCR a absence protilátek). Při fokální infekci můžeme najít v krvi jakýkoliv obraz, který se zpravidla mění v čase.
A nyní nutné intimnosti:
Antigen p27 je antigen, který je u infikovaných koček produkován v nadbytečném množství. Na jeho průkaz je možné využít dvě metody – ELISA nebo IFA. Metoda ELISA (nachází se v rychlotestech) detekuje solubilní p27, který je schopna zachytit v malém množství, zatímco IFA (imunofluorescence) detekuje antigen p27 vázaný na buňky. Pokud by to nebylo pro diagnostiku klíčové, vůbec bychom Vás těmito podrobnostmi nezatěžovali. Jelikož je však rozdílný výsledek testů diagnostický, musíme se v nich trochu orientovat. Pro zjednodušení malá tabulka:
| Metoda | ELISA | IFA |
| Detekuje | solubilní p27 | p27 vázaný zejm. na neutrofily a trombocyty |
| Výhody | více senzitivní, tj. zachytí malé množství antigenu; obsažena v rychlotestech | je specifičtější pro aktuální nemoc |
| Nevýhody | pozitivní výsledek nedeterminuje prognózu | kočka je infekční před pozitivním výsledkem |
| Pozitivita | během pár týdnů od infekce, určitě do měsíce od infekce | nejdříve za 3 týdny od infekce (po infikovaní kostní dřeně) |
| Pozitivní znamená | probíhá antigenemie, která může být ještě eliminována. Je nutné testovat kočku za 6 týdnů, a pokud je stále pozitivní za dalších 10 týdnů. Pokud bude stále pozitivní, s největší pravděpodobností má progresivní FeLV. Obecně je vhodné vzhledem k možnosti falešné pozitivity ihned otestovat kočku alespoň jiným ELISA testem. | má perzistentní viremii tj. na 91-97 % má progresivní FeLV |
| Falešně pozitivní test může být pokud | byla pro test použitá plná (nebo hemolyzovaná) krev, opakovat s plasmou nebo sérem; 1-2 % koček mají anti-myší protilátky (to není vtip!), které reagují s myšími složkami testu; jste špatně test promyli; byly pro test použity sliny nebo slzy | byl tlustý krevní náter; byla použita krev s antikoagulans; byl nezkušený personál (jedná se o mikroskopické hodnocení) |
| Falešně negatívní test může být pokud | byly pro test použity sliny nebo slzy; byl proveden příliš brzy | má kočka neutropenii nebo trombocytopenii (tj. není kde hledat antigen) |
| Pozitivní a negativní prediktivní hodnota | 80 % a téměř 100 %, tj. pozitivnímu výsledku věříme u 8 z 10 koček (zejména u koček, kde jsme to nečekali), negativní je v daný moment (snad) pravdivý |
Kromě antigenu p27 jsme schopni detekovat virovou RNA nebo provirus pomocí PCR. Metody PCR by mohly být pro detekci ideální – je možné je provést z jakéhokoliv vzorku a jsou velmi senzitivní, problémem je, že i kdyby test prováděl bezchybný personál (riziko kontaminace nebo technických potíží), retroviry rádi mutují a proto není jistota, že aktuálně používané primery budou relevantní (tj. mutované viry vyjdou negativně). Hlavní indikací provedení PCR je detekce regresivní FeLV u koček s tumory nebo jinými adekvátními příznaky, u kterých je replikace viru tak nízká, že jsou jiné testy negativní. Kvantitativní (real-time) PCR umožňuje odlišit mezi progresivní a regresivní infekcí dle „aktivity viru“. Další možností je stanovení PCR ze slin, kdy kočky s progresivní infekcí budou pozitivní, zatímco kočky s negativním výsledkem budou mít spíš regresivní infekci. Stabilita slin pro PCR je řádově v týdnech při pokojové teplotě.
Testování protilátek pro detekci aktuálního stavu zvířete není výtěžné, zdá se však, že na rozdíl od jiných infekcí, není pozitivní výsledek nejhorší možnou zprávou. Kočky s pozitivním titrem mohou spadat do následovných kategorií:
- vakcinovaná kočka,
- kočka s abortivní infekcí (tj. i úspěšně překonanou),
- kočka s regresivní infekcí
- kočka s atypickou infekcí
Z uvedeného vyplývá, že pozitivní FeLV protilátky neurčují prognózu. Ani z negativního výsledku se předčasně neradujme, kočky s progresivní infekcí mají většinou absenci FeLV protilátkové odpovědi, tj. negativní test mají:
- zdravé kočky,
- kočky s progresivní infekcí.
Alespoň jedna dobrá zpráva je, že kočky s pozitivními titry není již nutné vakcinovat. Z hlediska diagnostiky, pokud budeme mít opakovaně pozitivní ELISA test s opakovaně nedetekovatelnými FeLV protilátkami, se jedná pravděpodobně o progresivní infekci.
…určitě se nemůžete dočkat, až budete tyto výsledky interpretovat majitelům 🙂
Souhrn a doporučení
V rámci veterinární praxe budeme muset pravděpodobně zodpovědět několik dotazů majitelům FeLV pozitivních koček o rizicích spojených s onemocněním:
- kočky s pozitivním FeLV antigen testem se považují za kočky vylučující infekci,
- kočky s progresivní infekcí vylučují virus perzistentně,
- virus je vylučován slinami, a proto je pro přenos nutné zabránit těsnému kontaktu (krmení, pití, pečování o kočku),
- obvykle je postačující separovat kočky (pozitivní a negativní) do samostatných místností,
- pokud je pozitivní kočka odhalena za nějakou dobu soužití s negativními kočkami, je pravděpodobné, že kočky se již s virem setkali a jsou vůči němu imunní,
- FeLV negativní kočky je možné vakcinovat, zejména pokud majitel nesouhlasí s rozdělením koček,
- riziko, že negativní kočky budou pozitivní (pokud s kočkou předtím žily) je 10-15 %.
Pro infikované kočky je doporučeno:
- indoor chov,
- kontroly max. co 6 měsíců,
- při kontrolách se soustředíme na: mízní uzliny, ústní dutinu (stomatitida), srst (parazité, plísně), oftalmologické vyš. a změření hmotnosti. Rutinní hematologii, biochemii a vyšetření moči, příp. trusu opakujeme každý rok,
- je vhodné asymptomní kočky kastrovat, pro snížení stresu spojeného s pohlavním cyklem (chirurgické operace dobře tolerují),
- vakcinace proti FPV, herpesu a kaliciviru je vhodná každých 6 měsíců a neměla by být provedena modifikovanými živými vakcínami,
- vyvarovat se imunosupresní (pokud není jasná indikace bez jiné možnosti) a myelotoxické terapii, ideálně se vyvarovat imunosupresní terapii i u koček v domácnosti (budou náchylnější k infekci nebo výstupu z regresivní formy).
Relevantní terapeutické informace pro jednotlivé příznaky:
- leukemie a lymfomy jsou obvykle během 1-2 měsíců fatální, mohou být léčeny chemoterapií (remise u 47-75 % pacientů s lymfomem, 25 % s AML),
- alimentární lymfom má špatnou prognózu,
- terapií sarkomu je chirurgie a radioterapie.
Antivirová chemoterapie byla použita experimentálně a její použití v klinické praxi nebylo etablováno. Mezi používané látky patří: zidovudin, didanosin, zalcitabin, suramin, foscarnet, ribavirin.
V rámci imunomodulační terapie se nabízí tyto možnosti:
- lidský IFN-α – pro perorální a subkutánní podání. U perorálního podání je IFN-α v žaludku inaktivován a zničen, u subkutánního dochází ke vzniku neutralizačních protilátek, které cytokin zničí. Podání IFN-α je využíváno pro jeho vazbu na receptory v ústní dutině, kde stimuluje lokální lymfoidní tkáň s předpokladem celotělové odezvy. Dávka je 1-50 IU/kg každých 24 hodin (existuje řada protokolů např. 7 dní podávání – 7 dní pauza, i u PO podání je riziko vzniku protilátek za cca měsíc), vyšší dávky efekt nezvyšují. V rámci experimentálních podmínek je však efekt zejména v lepším klinickém stavu, než v potlačení viremie.
- kočičí IFN-ω má výhodu, že proti němu nevznikají protilátky. Terapeutický protokol 1×106 IU/kg q24h SC 5 dní po době v 5denních sériích (0., 14. a 60. den) prodloužil přežitelnost bez přítomnosti vedlejších účinků.
V rámci prevence je ve vztahu k vakcinaci vhodné zohlednit tyto informace:
- vakcinace neinterferuje s testování na FeLV pokud testování neprobíhá v krátkém čase po podání vakcíny,
- odpověď na vakcinaci není úplně homogenní,
- u FIV pozitivních koček není vakcinace proti FeLV úspěšná,
- vakcíny chrání proti viremii a onemocněními spojenými s FeLV, nechrání vůči integraci proviru a neposkytuje jistotu, že zvíře neonemocní,
- existují důkazy o spojitosti mezi vakcinací proti FeLV (a vzteklině) a rozvojem postinjekčního sarkomu (FISS, riziko méně než 1:10000, vzniká 4 měsíce až 2 roky po aplikaci, způsobují ho i jiné aplikace než vakcíny, doporučení prevence je aplikace vakcín do končetin – FeLV do Levé, vzteklinu (rabies) do pRavé, co nejdistálněji a přísně s.c.),
- je kontraindikovaná aplikace vakcín do interskapulární oblasti,
- preferujeme vakcíny s boostrem o tři roky.
Otázka epidemiologického rizika je vysoce nepravděpodobná. Virus sice není druhově specifický a existují nepřímé nálezy jeho „mezidruhové aktivity“, např. je schopný růst kulturách kostní dřeně lidí, u lidí (s leukemií nebo majitelů viremických koček) byli zaznamenány cirkulující FeLV protilátky, existuje studie naznačující vztah mezi kontaktem nemocné kočky a leukémii dětí (pouze na základě anamnézy). Na druhou stranu (a to je důležitější) nebyla prokázaná schopnost maligní transformace na buněčných liniích lidí. Zatím žádný člověk nebyl potvrzen jako viremický FeLV, PCR z krve a dřeně u dospelých a mladistvých s leukemií bylo negativní a doposud ani jeden případ leukemie lidí nebyl spojen s FeLV. Vysvětlením rozdílných „nálezů“ může být v lytické aktivitě komplementového systému člověka. Jelikož by byl zoonotický potenciál FeLV katastrofální, věnovala se této problematice opravdu velká řada studií. FeLV pozitivní kočky však není doporučeno držet v domácnosti s imunosuprimovanými osobami, a to z důvodu komorbidit, které mohou přenést.
Zdroje:
Hartmann K. In Greene CE (ed): Infectious Diseases of the Dog and Cat, ed 3, 2006, Elsevier, pp105-130.
Hartmann, K. Clinical aspects of feline immunodeficiency and feline leukemia virus infection. Veterinary Immunology and Immunopathology 2011, 143(3-4), 190–201. doi:10.1016/j.vetimm.2011.06.003
Loar, A. S. (1987). The Zoonotic Potential of Feline Leukemia Virus. Veterinary Clinics of North America: Small Animal Practice, 17(1), 105–115. doi:10.1016/s0195-5616(87)50608-8
Interpreting Unexpected Feline Leukemia Virus Test Results, ACVIM 2008, John R. August, BVetMed, MS, MRCVS, DACVIM
Pinches MDG, et al. J Fel Med Surg 2007;9:8.
J Vet Diagn Invest 8:25-30 (1996) Feline leukemia virus detection by ELISA and PCR in peripheral blood from 68 cats with high,moderate, or low suspicion of having FeLV-related disease Marion L. Jackson, Deborah M. Haines, Susan M. Taylor, Vikram Misra
Buch, J. S., Clark, G. H., Cahill, R., Thatcher, B., Smith, P., Chandrashekar, R., … Beall, M. J. (2017). Analytical validation of a reference laboratory ELISA for the detection of feline leukemia virus p27 antigen. Journal of Veterinary Diagnostic Investigation, 29(5), 654–659. doi:10.1177/1040638717710451
Feline Leukemia Virus Infection: Overview and New Developments World Small Animal Veterinary Association World Congress Proceedings, 2010 Hans Lutz, Dr.med.vet.habil.; Regina Hofmann, Dr.med.vet.habil.
Beatty, J. Viral causes of feline lymphoma: Retroviruses and beyond. The Veterinary Journal 2014, 201(2), 174–180. doi:10.1016/j.tvjl.2014.05.026
Hartmann, K. Clinical aspects of feline immunodeficiency and feline leukemia virus infection. Veterinary Immunology and Immunopathology 2011, 143(3-4), 190–201. doi:10.1016/j.vetimm.2011.06.003
Viruses. 2012 Nov; 4(11): 2684–2710. Clinical Aspects of Feline Retroviruses: A Review. Katrin Hartmann
Interpreting Unexpected Feline Leukemia Virus Test Results, ACVIM 2008, John R. August, BVetMed, MS, MRCVS, DACVIM
Willett, B. J., & Hosie, M. J. (2013). Feline leukaemia virus: Half a century since its discovery. The Veterinary Journal, 195(1), 16–23. doi:10.1016/j.tvjl.2012.07.004
Schweiz Arch Tierheilkd. 2018 Feb;160(2):95-105. doi: 10.17236/sat00146. Feline leukemia virus infection: importance and current situation in Switzerland.Hofmann-Lehmann R, Gönczi E, Riond B, Meli M, Willi B, Howard J, Schaarschmidt-Kiener D, Regli W, Gilli U, Boretti F
